高球蛋白血症会有什么危害 高球蛋白血症背后的病因探查
*仅供医学专业人士阅读参考

球蛋白水平异常增高可能由哪些原因造成,怎么治疗?
球蛋白由机体免疫器官生成,其含量反映了机体的体液免疫功能状态。高球蛋白血症是指血清球蛋白浓度超过35g/L,其背后成因复杂,球蛋白水平的异常升高也可能是多种疾病的临床早期异常表现。临床中遇到球蛋白水平显著升高可能在向我们传达有关身体状况的重要讯息,在诊疗中不可大意,以免延误病情。
本期,重庆医科大学附属第二医院任飞凤医生为我们带来一例患有高球蛋白血症的患者的诊疗经过,重庆医科大学附属第二医院唐琳教授将就本案例进行点评。
案例资料
▎基本情况:患者女,54岁。
▎主诉:发现肝功能不全3年、鼻衄2月,于2021年1月11日入住我科。
▎现病史:3年前患者因头晕就医时生化提示肝功能异常,肝酶较正常上限升高10倍,外院肝穿活检结果提示“自身免疫性肝炎”,反复保肝治疗;2月前患者无明显诱因反复出现鼻衄伴牙龈出血,对症止血治疗后好转;后渐出现口干、咽干和脱发。10天前患者就诊我院血液科查凝血酶原时间(PT)、活化部分凝血活酶时间(APTT)轻度延长,纤维蛋白原(Fib)轻度降低,谷丙转氨酶(ALT)116 U/L,谷草转氨酶(AST)132 U/L,碱性磷酸酶(ALP)176 U/L,抗核抗体(ANA)1:100,抗SSA、SSB、Ro-52、AMA-M2抗体阳性,IgG 67 g/L,IgA 4.39 g/L,凝血因子活性检测:Ⅶ42%,Ⅻ41%,Ⅺ31%,Ⅸ39%,Ⅷ152%,Ⅹ57%,Ⅴ62%,Ⅱ62%,血管性血友病因子抗原267%,为进一步诊治就诊我科。
▎既往史:1年前反复“荨麻疹”。
▎入院查体:体温(T)36.8℃,脉搏(P)80次/分,呼吸(R)20次/分,血压(BP)140/64 mmHg。无皮疹,无淋巴结肿大,心肺腹部未发现异常,双下肢无凹陷性浮肿,病理征阴性。
▎辅助检查:
-
血常规:血红蛋白(Hb)107 g/L↓,白细胞计数(WBC)2.9×109/L↓,血小板计数(PLT)104×109/L。
-
肝功能:总蛋白(TP)97 g/L↑,白蛋白28 g/L↓,球蛋白(GLB)68 g/L↑,ALT 98 U/L↑,AST 109 U/L↑,ALP 188 U/L↑,前白蛋白(PA)65 mg/L↓,总胆汁酸(TBA)34 μmol/L↑
-
尿常规、大便常规正常。
▎凝血功能检查:PT 17.3s↑、APTT 47s↑,Fib 1.84 g/L↓;凝血因子Ⅷ152%,血管性血友病因子抗原267%。提示肝细胞合成功能异常。
▎炎症、感染方面检查:红细胞沉降率(ESR)65 mm/h↑,余无异常。
▎肝硬化、肿瘤方面检查:
-
甲胎蛋白(APF)90.77(正常范围0-13)。
-
肝纤谱:透明质酸、层粘连蛋白升高1倍;Ⅳ型胶原升高3倍。
-
消化道标志物:CA125/199/724/50/242均未见异常。
-
血尿免疫固定电泳:未见单克隆、寡克隆免疫球蛋白。
▎免疫检查:
-
抗可提取核抗原抗体(抗ENA):抗SSA抗体 ,抗SSB抗体 ,抗Ro-52抗体 。
-
自免肝抗体谱:ANA 1:100胞浆颗粒型;抗AMA-M2抗体83.2。
-
免疫球蛋白:IgG 67.3 g/L↑,IgA 4.39 g/L↑,Igκ 14.6 g/L↑,Igλ 4.81 g/L↑,IgG4正常。
-
补体:C3 0.82 g/L↓,C4 0.04 g/L↓
-
自身抗体:类风湿因子(RF)、抗环瓜氨酸肽抗体(抗CCP抗体)、抗角蛋白抗体(AKA)、抗突变型瓜氨酸波形蛋白抗体(抗MCV)、抗中性粒细胞胞浆抗体(ANCA)阴性;抗心磷脂抗体(ACL)、抗β2糖蛋白1(β2GP1)抗体和狼疮抗凝物(LA)均阴性。
-
直接Coombs试验1 。
▎影像学检查:
-
涎腺彩超:双侧颌下腺体积变小、回声不均质;腮腺未见异常。
-
甲状腺彩超:左侧叶胶质囊肿。
-
胸部CT平扫:肺部实性微结节,未见间质性肺病(ILD)。
-
骨密度:骨质疏松。
-
鼻内镜检查:李氏区糜烂,鼻粘膜苍白,易糜烂出血。
▎骨髓检查:涂片:粒系增生欠佳,成熟加速;活检:骨髓增生活跃。
▎眼科检查:
-
Schirmer试验:右4mm/5min,左5mm/5min。
-
泪膜破裂时间(BUT):右3s,左4s。
-
角膜染色:阴性。
-
眼底、视野、视神经未见异常。
▎诊断:
1、重叠综合征
自身免疫性肝炎(AIH)
干燥综合征(SS)
原发性胆汁性肝硬化(PBC)
2、高球蛋白血症(AIH、SS)
3、甲状腺胶质囊肿
4、骨质疏松
5、鼻出血
▎治疗:甲泼尼龙16 mg qd,羟氯喹200 mg bid,艾拉莫德25 mg bid,熊去氧胆酸胶囊250 mg tid,双环醇25 mg tid,护胃、抗骨质疏松治疗。
▎随访:
-
治疗1月后,血常规、ESR、凝血功能、转氨酶水平恢复正常;
-
肝功能好转:转氨酶恢复正常,GLB水平显著下降;
-
免疫球蛋白:球蛋白及IgG水平随治疗时间的延长而持续降低,目前已恢复正常(图1);
-
患者未再鼻出血,无明显不良反应发生。
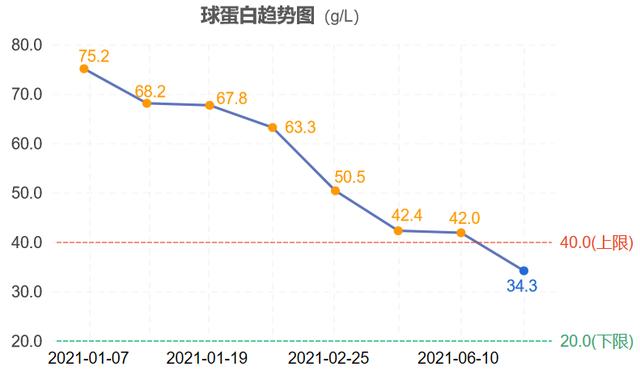

图1:治疗期间,球蛋白和免疫球蛋白IgG水平变化
专家点评
临床中,高球蛋白血症常与急慢性感染、恶性肿瘤、自身免疫疾病、慢性肝病及浆细胞病相关,但确切病因尚不清楚[1]。高球蛋白血症本身并不引起任何症状,患者的大多数症状与其原发疾病有关,可为原发疾病的诊断提供重要线索[2-3]。免疫球蛋白水平的升高可造成较大危害,常引起血液粘滞性增加、微循环障碍及组织器官的缺血缺氧,最终导致组织器官损害[4],临床中应予以重视和及时干预。
免疫球蛋白是由重链和轻链组成的蛋白质,其类别主要以重链中的恒定区来定义。不同类别免疫球蛋白水平的升高可能提示不同的疾病。如,IgG浓度的升高与肝脏疾病、自身免疫性/炎症性疾病、血管炎、感染、血液学障碍、非血液学的恶性肿瘤、免疫缺陷等密切相关;IgM浓度的增加通常与B细胞免疫球蛋白类别转换受损有关;IgA浓度增加最常见原因为肝硬化,当然也常见于IgA肾病、IgA血管炎和部分自身免疫性疾病;IgD的升高与高IgE综合征相关;血清IgE浓度升高常发生在各种过敏性和特应性疾病、淋巴瘤和高IgE综合征[3]。
其中,IgG是表达最为丰富的免疫球蛋白,大部分高球蛋白血症表现为IgG水平的升高。IgG由B淋巴细胞在抗原刺激下转化为浆细胞后产生,在免疫过程中起着重要作用,包括补体的激活和调理作用[3]。活化的B淋巴细胞可产生大量多克隆自身抗体,抗原抗体复合物激活补体系统,可引起补体成分C3和C4下降[1]。本例患者凝血功能和肝功能异常,多个类别免疫球蛋白浓度升高(以IgG的升高最为显著)且补体水平降低,具有明显的高球蛋白血症,为控制病情,需仔细探查其背后病因。
通过全面检查,包括临床症状与体征、实验室生化及免疫检查、血清学检测、组织病理检测和影像学检查以及专科检查(如眼科)等,患者符合2010年美国肝病学会提出的AIH诊断标准[5]、2021年中华医学会肝病学分会提出的PBC的诊断标准[6]以及2016年美国风湿病学会/欧洲抗风湿病联盟提出的SS分类标准(血清抗SSA抗体阳性 至少单眼Schirmer试验≤5 mm/5 min)[7],因此被诊断为同时存在AIH、PBC以及SS的重叠综合征,而AIH和SS均可引发高球蛋白血症。
高球蛋白血症并没有特异性治疗方法,其治疗主要针对原发疾病。在大多数情况下,原发疾病的治疗可缓解免疫失调和异常炎症反应,从而导致高球蛋白血症的消退[3]。艾拉莫德(IGU)是一种多靶点的新型免疫调节剂,可调节细胞及体液免疫,抑制B细胞的活化,降低免疫球蛋白的分泌[8]。
在各种探索IGU对SS治疗疗效的研究中,IGU表现出巨大潜力,有效降低SS患者的ESSDAI评分和多种免疫球蛋白水平,对SS伴发的高免疫球蛋白血症有一定的治疗效果[9-11]。而对于AIH,其组织学特征是淋巴细胞、浆细胞和巨噬细胞的密集浸润,就目前所发现的分子发病机制而言,Treg细胞数量及功能受损似乎在其中发挥了重要作用[12],而球蛋白水平的升高则与B细胞相关,因此IGU对细胞及提体液免疫的调节作用或许对AIH的治疗也有一定的益处。
在本例患者的治疗方案中,糖皮质激素(甲泼尼龙)是AIH的一线治疗方案,其对SS活动系统性病变的控制亦有显著疗效。而IGU则可发挥改善SS相关症状,降低免疫球蛋白水平的疗效。在治疗中,患者的炎症指标(ESR)、血常规及凝血功能、肝功能均恢复正常,免疫球蛋白IgG显著下降,原发疾病的相关症状好转,证明了此治疗方案的有效性及安全性。
专家简介

唐琳 教授
重庆医科大学附属第二医院内科教研室主任、风湿免疫科主任、博士、博士研究生导师
-
重庆英才•创新领军人才
-
重庆市风湿与临床免疫学学术技术带头人
-
中国医师协会风湿免疫科分会全国委员
-
重庆市医学会风湿病分会副主任委员
-
重庆市医师协会风湿病专业委员会副会长
-
重庆市医学会罕见病分会副主任委员
-
重庆市中西医结合学会风湿疾病专业委员会副主任委员
-
海峡两岸医药卫生交流协会风湿免疫病学专业委员会眼免疫学组委员
专家简介

任飞凤
-
重庆医科大学附属第二医院主治医师
-
重庆市医学会风湿病学分会青年委员会副主任委员
-
以第一作者发表SCI文章4篇,在《Rheumatology》上发表论文2篇,单篇最高影响因子7.58分
参考资料:
[1]苏延军,胡小军,李改英,等.高球蛋白血症268例鉴别诊断[J].中国现代医药杂志.2017,19(5):58-60.
[2]Rasel M,Zahra F. Hypergammaglobulinemia(Polyclonal Gammopathy)[Updated 2022 Sep 23]. In:StatPearls[Internet]. Treasure Island(FL): StatPearls Publishing; 2022 Jan-.Available from: https:// www.ncbi.nlm.nih. gov/books/NBK585137/
[3]Zhao EJ,Cheng CV,Mattman A, et al. Polyclonal hypergammaglobulinaemia: assessment,clinical interpretation, and management[J].Lancet Haematol. 2021,8(5): e365-e375.
[4]杨丹丹,张杰.高球蛋白血症性紫癜并发原发性干燥综合征一例[J].中国麻风皮肤病杂志,2019,35(2):92-95.
[5]Manns MP,Czaja AJ,Gorham JD,et al. Diagnosis and management of autoimmune hepatitis[J]. Hepatology.2010,51(6):2193-213.
[6]中华医学会肝病学分会.原发性胆汁性胆管炎的诊断和治疗指南(2021)[J].临床肝胆病杂志,2022,38(1):35-41.
[7]Shiboski CH,Shiboski SC,Seror R,et al.2016 American College of Rheumatology/European League Against Rheumatism classification criteria for primary Sjögren's syndrome:A consensus and data-driven methodology involving three international patient cohorts[J].Ann Rheum Dis.2017,76(1):9-16.
[8]Yan Y,Mei L,FuYe Q,et al. Iguratimod represses B cell terminal differentiation linked with the inhibition of PKC/EGR1 axis[J].Arthritis Research&Therapy. 2019,21:92.
[9]王雪,袁祥,王其凯,等.艾拉莫德对原发性干燥综合征的治疗作用及其机制[J].中华疾病控制杂志.2018,1:75-78.
[10]Chen H,Qi X,Li Y,et al.Iguratimod treatment reduces disease activity in early primary Sjögren's syndrome: An open-label pilot study[J].Mod Rheumatol. 2021,31(2):394-398.
[11]Jiang W,Zhang L,Zhao Y,et al.The efficacy and mechanism for action of iguratimod in primary Sjögren's syndrome patients[J].Int Ophthalmol. 2020,40(11):3059-3065.
[12]Manns MP,Lohse AW,Vergani D. Autoimmune hepatitis--Update 2015[J]. J Hepatol.2015,62(1 Suppl): S100-11.
此文仅用于向医疗卫生专业人士提供科学信息,不代表平台立场。

免责声明:本文仅代表文章作者的个人观点,与本站无关。其原创性、真实性以及文中陈述文字和内容未经本站证实,对本文以及其中全部或者部分内容文字的真实性、完整性和原创性本站不作任何保证或承诺,请读者仅作参考,并自行核实相关内容。文章投诉邮箱:anhduc.ph@yahoo.com






