so3的立体构型及共价键类型(基于MS的Dmol3模块计算离子液体的电子转移和成键)
离子液体是由氢键供体(HBDs)和氢键受体(HBAs)按照一定比例混和组成的低共熔混合物,常温下呈液态。氯化胆碱由于其价格低廉、来源广泛、可生物降解等特点成为了最常用的氢键受体之一,形成了一系列胆碱类离子液体。在吸收有害气体、生物质催化转化、电沉积、功能材料制备等工业领域已经得到广泛应用。
因此,本文以氯化胆碱离子对为模型,在量子力学基础上系统的研究氯化胆碱离子对之间的的电子转移和成键情况,从而为这种以氢键相结合的胆碱类离子液体更广范应用提供理论依据。在Material Studio 2019软件包下的Dmol3模块计算氯化胆碱离子对模型,计算参数为GGA广义梯度近似和BLYP泛函方法,在计算精度为Medium的基础上选择DND 4.4基组,体系总能量收敛值取 2.0X10-5eV/atom。计算的能量通过基组重叠误差(Basis Set Superposition Errors,BSSE)进行校正。首先,通过Visualizer面板画出氯化胆碱离子对模型(图左),然后用Dmol3模块进行优化计算,得到能量最低构型(图右)。然后计算其前线分子轨道、态密度等电子性质。

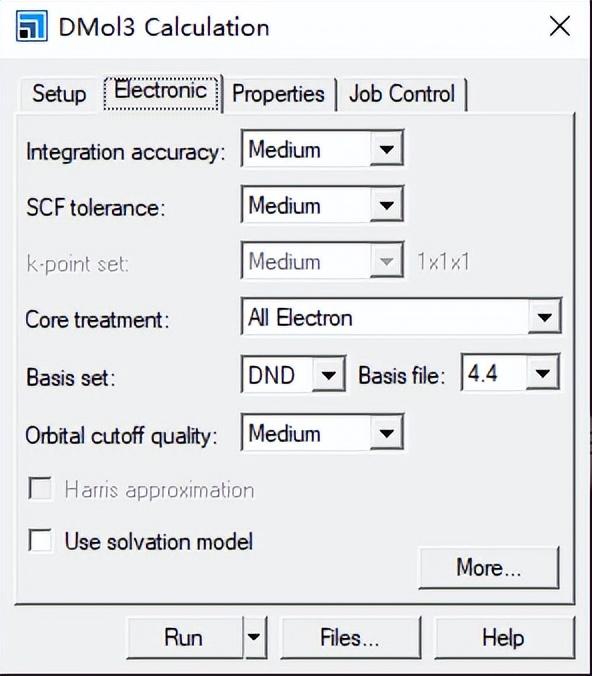


计算面板


分析面板


优化前 优化后
氯化胆碱离子对




Ch HOMO轨道 Ch LUMO轨道 Cl- HOMO轨道 Cl- LUMO轨道
根据前线分子轨道理论,参加反应的两种物质的最高占据轨道(HOMO)和最低空轨道(LUMO)能量越接近,越容易发生反应。通过计算ΔE获得具体数值,其中ΔE=|LUMO-HOMO|,ΔE越小,越容易发生HOMO→LUMO的电子转移,相互作用越强,获得的产物越稳定。通过计算发现胆碱阳离子的LUMO轨道与氯离子的HOMO轨道之间ΔE更小,而且两个数值更接近,这说明了在氯化胆碱成键过程中的电子是由氯离子向胆碱阳离子转移的。



(a)总态密度图 (b)分波态密度 (c)游离态分波态密度
由图(a)可知Chcl的最高占据态为-1~0.5Ha,在这一范围内胆碱阳离子比氯离子贡献较多,主要是由于胆碱阳离子内存在四个氢键供体,而氯离子只是一个氢键受体。通过图3(b)可以看出氯离子与氧、碳原子发生强烈共振,在最高占据态内是由Cl-3s、Cl-3p、O2s、O2p、C22s、C22p、C42s、C42p、C52s、C52p贡献,其中Cl-3p、O2p、C22p、C42p、C52p占主导地位,说明形成的p-p杂化轨道是阴阳离子间电子转移的主要通道。同时通过对比图 (b)、(c),可以出氯化胆碱中的各个轨道向低能方向移动程度比较小,再次证明了形成的多重氢键键能较弱。
最后,有相关需求欢迎通过公众号联系我们。
公众号:320科技工作室
,免责声明:本文仅代表文章作者的个人观点,与本站无关。其原创性、真实性以及文中陈述文字和内容未经本站证实,对本文以及其中全部或者部分内容文字的真实性、完整性和原创性本站不作任何保证或承诺,请读者仅作参考,并自行核实相关内容。文章投诉邮箱:anhduc.ph@yahoo.com






