高中化学必修一氧化还原反应重点(高考化学一轮提分练)
1.(2017·葫芦岛六校协作体高三上学期期初考试)将浓盐酸滴入KMnO4溶液,产生黄绿色气体,溶液的紫红色褪去,向反应后的溶液中加入NaBiO3,溶液又变为紫红色,BiO3(-)反应后变为无色的Bi3+。据此判断下列说法正确的是( )
A.滴加盐酸时,HCl是还原剂,Cl2是还原产物
B.已知Bi为第ⅤA族元素,上述实验说明Bi具有较强的非金属性
C.若有0.1 mol NaBiO3参加了反应,则整个过程转移电子0.4NA
D.此实验条件下,物质的氧化性:KMnO4>NaBiO3>Cl2
2.(2017·成都七中高三零诊)在酸性介质中,往MnSO4溶液里滴加(NH4)2S2O8溶液会发生如下离子反应(未配平):Mn2+ +S2O8+H2O―→MnO4(-)+SO4(2-)+H+,下列说法不正确的是( )
A.氧化性比较:S2O4(2-)>MnO4(-)
B.氧化剂S2O8(2-)的摩尔质量为192 g·mol-1
C.该反应中酸性介质可以为盐酸
D.若有0.1 mol氧化产物生成,则转移电子0.5 mol
3.已知酸性高锰酸钾溶液可以氧化FeSO4,反应的化学方程式为2KMnO4+10FeSO4+8H2SO4===K2SO4+X+5Fe2(SO4)3+8H2O,现将一定量的硫酸酸化的高锰酸钾溶液与硫酸亚铁溶液混合,充分反应后再向所得溶液中加入KI溶液(假设I-与KMnO4反应的氧化产物为I2),混合溶液中铁离子的物质的量随加入的KI的物质的量的变化关系如图所示。则下列有关说法不正确的是( )

A.方程式中的X为2MnSO4
B.氧化性:KMnO4>Fe3+>I2
C.根据OC段的数据可知开始加入的高锰酸钾的物质的量为0.30 mol
D.AB段是高锰酸钾和碘化钾溶液反应,BC段的反应为2Fe3++2I-===2Fe2++I2
4.(2017·银川一中高三第一次月考)已知某一反应体系有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。已知该反应中H2O2只发生如下过程:H2O2→O2,则关于该反应体系说法错误的是( )
A.该反应的化学方程式为2H2CrO4+3H2O2===2Cr(OH)3↓+3O2↑+2H2O
B.该反应中的氧化剂是H2O2,还原产物是O2
C.氧化性:H2CrO4>O2
D.如反应转移了0.3 mol电子,则产生的气体在标准状况下体积为3.36 L
5.(2017·石家庄二中高三上学期第二次联考)用高铁酸钠(Na2FeO4)对河、湖水消毒是城市饮用水处理的新技术,已知反应:Fe2O3+ 3Na2O2===2Na2FeO4+Na2O。下列说法正确的是( )
A.Na2O2既是氧化剂又是还原剂
B.Fe2O3在反应中显氧化性
C.1 mol Na2O2发生反应,有4 mol电子转移
D.Na2FeO4能消毒杀菌是因其具有强氧化性
6.(2017·衡阳八中高三月考)根据如图的转化关系,判断下列说法正确的是(反应条件已略去)( )
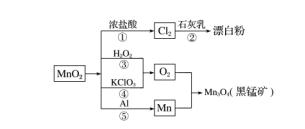
A.反应①②③④⑤均属于氧化反应和离子反应
B.反应⑤说明该条件下铝的还原性强于锰
C.相同条件下生成等量的O2,反应③和④转移的电子数之比为1∶1
D.反应①中氧化剂与还原剂的物质的量之比为1∶4
7.已知氧化性:BrO3(-)>ClO3(-)>Cl2>IO3(-)>I2。现将饱和氯水逐滴滴入KI淀粉溶液中至过量。
(1)可观察到的现象是
①________________________________________________________________________;
②________________________________________________________________________。
(2)写出有关反应的离子方程式:
①________________________________________________________________________;
②________________________________________________________________________。
8.高锰酸钾分别在酸性、中性、碱性条件下发生的反应如下:
MnO4(-)+5e-+8H+===Mn2++4H2O
MnO4(-)+3e-+2H2O===MnO2↓+4OH-
MnO4(-)+e-===MnO4(2-)(溶液呈绿色)
(1)从上述三个半反应中可以看出高锰酸根离子被还原的产物受溶液的____________影响。
(2)将SO2通入高锰酸钾溶液中,发生氧化还原反应的离子方程式为________________________________________________________________________。
(3)将PbO2投入酸性MnSO4溶液中搅拌,溶液变为紫红色。下列说法正确的是________(填字母)。
a.氧化性:PbO2>KMnO4
b.还原性:PbO2>KMnO4
c.MnSO4溶液可以用盐酸酸化
,免责声明:本文仅代表文章作者的个人观点,与本站无关。其原创性、真实性以及文中陈述文字和内容未经本站证实,对本文以及其中全部或者部分内容文字的真实性、完整性和原创性本站不作任何保证或承诺,请读者仅作参考,并自行核实相关内容。文章投诉邮箱:anhduc.ph@yahoo.com






