初中化学1至4单元经典易错题(4单元易错点习题练习)

今天给大家分享初中化学1~4单元的易错知识点,看看你都会了吗?一、化学用语
1.回答下列问题:
(1)NaNO2中N元素的化合价为 。
(2)由N、H、Cl三种元素组成的一种盐的化学式是 。
(3)从分子的角度分析,做饭时间到饭菜的香味,是因为 。
(4)CO2中“2”表示的意义是 。
【答案】(1)NaNO2中N元素的化合价为 3。
(2)由N、H、Cl三种元素组成的一种盐的化学式是 NH4Cl。
(3)从分子的角度分析,做饭时间到饭菜的香味,是因为 分子在不断的运动 。
(4)CO2中“2”表示的意义是 每个二氧化碳分子中含有2个氧原子 。
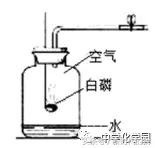
2.(2018·江西)(4分)根据下图,将下列带点的部分用化学用语填空:
(1)空气中氮气的化学式_______________;
(2)瓶中物质燃烧的化学方程式________________________;
(3)瓶中的水吸收白烟生成偏磷酸(HPO3),偏磷酸中磷元素显 5价___________。
【答案】(1)N2;(2) 4P 5O2=(点燃)2P2O5 (3)
3(2018·甘肃)俄罗斯方块你玩过吗?下面是为你设计的化学俄罗斯方块,请根据示例写出下列“口"中对应的化学符号或符号所表达的含义。
【答案】(1)2NH 4 + (2)3个二氧化硫分子 (3)Fe
2
Cl2
二、写出化学方程式
(1)碳的燃烧 ;
(2)硫的燃烧 ;
(3)铁丝的燃烧 ;
(4)红磷的燃烧 ;
(5)汞和氧气反应 ;
(6)氧化汞加热分解 ;
(7)镁和氧气反应 ;
(8)铝和氧气反应 ;
(9)高锰酸钾分解制取氧气 ;
(10)氯酸钾分解制取氧气 ;
(11)过氧化氢分解制取氧气 ;
(12)水的通电分解 ;
(13)氢气燃烧 。
三、空气
1.下列关于O2的说法中,正确的是 ( )
A. O2的重要用途是供给呼吸和作燃料
B. 可用带火星的木条来检验空气中是否含有O2
C. 用过氧化氢溶液制O2,必须用MnO2作催化剂
D. 工业上可利用液态氮和液态氧的沸点不同从空气中制取O2
【答案】D
2.下列物质在氧气中燃烧的现象正确的是( )
A.红磷燃烧产生白雾,放出大量热
B.铁丝燃烧火星四射,放出大量热,生成黑色固体
C.木炭燃烧生成二氧化碳,该气体能使澄清石灰水变浑浊
D.硫燃烧发出淡蓝色火焰,放出大量热,生成有刺激性气味的气体
【答案】B
3.下图是测定空气中氧气含量的实验装置图,回答下列问题:
(1)集气瓶里预先放少量的水的目的除了吸热还有 的作用。
(2)燃烧匙内盛放的物质是 (填序号);
A.红磷 B.铁丝 C.木炭 D.硫磺
(3)燃烧的过程中观察到的现象是 ;
打开止水夹看到的现象是 ;
得出的主要结论是 ;
还能推出氮气的物理性质是 ;
氮气的化学性质是 ;
(4)下列事实中,会导致测量结果偏低的是 ;
A.装置气密性不好 B.红磷量不足 C.将红磷换成白磷 D.未冷却到室温就读数
E.止水夹没夹紧 F.燃着的红磷没有迅速插入集气瓶中
【答案】用红磷在集气瓶燃烧测定空气成分的实验中,集气瓶中预先放少量水的目的是为了吸收五氧化二磷,并降低装置温度 防止集气瓶底炸裂;A;产生白烟,放出大量热;烧杯内的水进入集气瓶中约占集气瓶体积的1/5;氧气约占空气体积的1/5;氮气难溶于水;氮气不能燃烧、也不支持燃烧;ABD。
4.在由两个注射器组成的密闭系统中留有25mL 空气,给装有细铜丝的玻璃管加热,同时缓慢推动两个注射器活塞,至玻璃管内的铜丝在较长时间内无进一步变化时停止加热,待冷却至室温,将气体全部推至一个注射器内,观察密闭系统内空气体积变化。(已知铜加热时颜色变黑,生成氧化铜)
(1)在实验加热过程中,交替缓慢推动两个注射器的目的是 ;
(2)写出该实验中反应的化学方程式 ;
(3)小强测得实验结果如下:
反应前注射器内气体总体积
反应后注射器内气体总体积
25mL
22mL
由此数据可以推算出他测定的空气中氧气的体积分数 2l%(填“>”、“=”或“<”)。造成该实
验出现误差的原因可能是 (填序号)。
①没有交替缓缓推动两个注射器活塞; ②读数时没有冷却至室温;
③加入铜丝量太少; ④加入铜丝量太多
【答案】使氧气与铜丝充分接触/使空气中的氧气充分与铜发生反应;2Cu O2=(△)2CuO;<;①②③
四、物质的分类 化学反应基本类型
【答案】B
2.(2018·甘肃)分类是学习化学的重要方法。下列物质属于氧化物的是( )
A.O2 B. H2 O C.KCl D.H2SO4
【答案】B
3、(2018·江西)硫在物质的分类中属于( )
A.混合物 B.化合物 C.非金属单质 D.金属单质
【答案】C
4、(2018·江西)下列“水”能使无色酚酞溶液变红的是( )
A.氨水 B.汽水 C.冰水 D.糖水
【答案】A
五、化学实验基本操作
【答案】B
2.(2018·泰州)下列实验操作错误的是( )
【答案】B
3.下列实验仪器的用途及使用注意事项中,正确的是( )
A. 酒精灯:加热,使用后应吹灭并盖上灯帽
B. 量筒:测量液体体积,不能被加热
C. 胶头滴管:吸取液体管口应向上,防止液体流出
D. 托盘天平:称量药品,药品直接放置在托盘上
【答案】B
4.某同学用量筒量取液体,读数面对刻度线,第一次仰视凹液面的最低处,读数为19mL,倒出部分液体后,又俯视读数为11mL,则倒出液体体积为( )
A.8mL B.小于8mL C.大于8mL D.无法判断
【解析】仰视凹液面最低处读数为19mL,实际体积大于19mL;倒出部分后,俯视凹液面最低处读数为11mL,此时量筒内液体的实际体积小于11mL,所以(>19ml)﹣(<11mL)=(>8 mL);故选C.
【点评】量取液体读数时,眼睛应平视,否则“高看偏高”,即从高处看,读数偏高;“低看偏低”即从低处看读数偏低.
广告
嗝嗝老师主演:拉妮·玛克赫吉 / 内拉吉·卡比 / 苏普丽雅·皮尔加卡尔
猫眼电影演出
六、物质构成的奥秘
1、(2018·江西)氧气在降温加压变成液态氧的过程中,下列说法正确的是( )A. 分子之间的间隔变小 B.分子质量变小
C.分子体积变大 D.分子运动速率变大
【答案】A
2.(2018·四川)已知元素周期表中第三周期各元素原子结构示意图如下,下列分析错误的是( )
A.以上原子的核外都有三个电子层
B.Na 和Mg2 的核外电子数不相同
C.Na与S形成化合物的化学式为Na2S
D.在化学反应中氯原子容易得到电子
【答案】B
3.(2018·江西)(6分) 2018年5月9日,我国“高分五号”卫星发射成功。
(1)高氯酸钾(KClO4) 可用作火箭燃料,其中氯元素的化合价为_________________。
(2)“高分五号”用钛镍形状记忆合金制作卫星天线。下图是镍元素在元素周期表中的信息以及原子结构示意图。镍元素的相对原子质量为_____________。X的数值是_____。
(3)“高分五号”是我国首颗对大气中二氧化硫,二氧化氮、二氧化硫,甲烷等多个环境要素进行监测的卫星。
①上述四种气体可以造成酸雨的是____________(写一种即可):
②催化还原法是消除大气中氮氧化物污染的新工艺,主要的微观示意图如下。下列说法正确的是___________(填序号)。
A.反应前后分子的种类不变
B.反应前后原子的种类发生改变
C.反应前后元素化合价都不变
D.反应后丁,戊的分子个数比为2: 1
【答案】(1) 7 (2) 58.69,2 (3) ①二氧化硫或二氧化氮;②D
4.下列关于NaNO2、Na2O2、SO2、O2等四种物质的组成的叙述中正确的是( )
A. 都含有氧气 B. 都含有氧元素
C. 都含有氧分子 D. 都含有2个氧原子 E.都含有氧单质
【答案】B
5.请从微观角度回答下列问题:
(1)体温计量体温时水银柱会升高,微观解释为 ;
(2)气态氧气和液态氧气化学性质相同的微观原因是 ;
(3)水和过氧化氢的化学性质不同,是因为它们的 不同;
(4)水的蒸发属于物理变化是因为 ;
(5)水的电解得到氢气和氧气,属于化学变化是因为 ;
(6)空气和氧气的区别 ;
(7)元素种类不同:是因为 不同;
(8)钠原子和钠离子属于同种元素的原因是 ,两者的化学性质不同是因为
;在“化学反应中的原子不变”是指原子中的 (选填“原子核”或“核外电子”)不变。
【答案】(1)体温计量体温时水银柱会升高,微观解释为 原子间有间隔 ;(2)气态氧气和液态氧气化学性质相同的微观原因是 同种分子性质相同 .(3)分子构成.(4)水蒸发变成水蒸汽,水分子未发生改变是,水分子的间隔发生了变化,是物理变化 (5) 水分子发生了变化,生成氢气分子和氧气分子,是化学变化;(6)空气和氧气的区别 空气中含有多种分子,氧气中只有一种氧分子 .(7)质子数不同;(8)质子数相同,最外层电子数目不同.原子核。
七、化学式的相关计算
1.(2018·浙江)茶叶中含有茶氨酸(C7H14O3N2),茶氨酸中各元素质量分数如图所示。其中①表示的元素是( )
A.碳 B.氢 C.氧 D.氮
【答案】A
2.(2018·浙江)我国用新技术提纯了稀有金属铼(Re),为航空航天发动机核心部件的制造提供了重要原料.
(1)铼原子的相对原子质量为186,原子核内有75个质子,则其核外电子数为_____。
(2)高铼酸钠(NaReO4)是铼的重要来源之一,高铼酸钠中铼元素的化合价为_____。
【答案】(1)75;(2) 7;
3.(2018·甘肃)(4分)生活中处处有化学。请按要求回答下列问题。
(1)自来水厂对天然水净化处理得到自来水的过程中,下列操作:①过滤②吸附③消毒④蒸馏,其中没有用到的是 (填序号)。
(2)用自来水烧水的水壶底部,容易形成水垢,水垢的主要成分是碳酸钙和氢氧化镁,可以用厨房中的一种调味品来潸除,这种调味品是 ;
(3)为防止人体缺碘,市售食盐中添加了少量的碘酸钾(KIO3),并在使用说明中强调“不
宜高温烹煮”。碘酸钾与氯酸钾化学性质相似,请写出碘酸钾在加热条件下分解的化学方程式
【答案】(1)④ (2)醋 (3)2KIO3 △ 2KI 3O2 ↑
4.(2018·甘肃)(2分)断血流滴丸主含有木犀草素(化学式为C15H10Ox,)等黄酮类活性成分,具有止血、抗菌、抗炎及免疫等药理活性。已知木犀草素的相対分子质量为286,请计算
(1)x的值为
(2)木犀草素中碳元素的质量分数为 (结果精确到0.1%)
【答案】(2分)(1)6(1分) (2)62.9% (1分)
5. 下列原子团的名称、符号、化合价都正确的是( )
A.硝酸根 NO3- -1价 B.铵根 NH3 1价
C.氢氧根 HO- -1价 D.硫酸根 H2SO4 0价
【答案】A
八.分析推理选择题(综合应用)
1.分析推理是化学学习中最常用的思维方法,判断对错
(1) 分子、原子是不显电性的粒子,但不显电性的粒子不一定是分子和原子(√)
(2) 离子都带有电荷,所以带电荷的粒子一定是离子 (×)
(3) 单质中只含有一种元素,所以由一种元素组成的纯净物一定是单质 (√)
(4) 单质中只含有一种元素,所以由一种元素组成的物质一定是单质 (×)
(5) 化合物是由不同种元素组成的纯净物,所以由不同种元素组成的纯净物不一定是化合物 (×)
(6) 因为H2O和H2O2的组成元素相同,所以他们的化学性质相同 (×)
(7) 因为蜡烛燃烧生成CO2和H2O,所以蜡烛组成里一定含有碳元素和氢元素(√)
(8) 氢、氧元素的本质区别是电子数不同(×)
(9) 金刚石和石墨物理性质不同是由于碳原子排列方式不同(√)
(10) 一氧化碳和二氧化碳的化学性质不同是由于它们的分子构成不同(√)
(11) 因为金属元素的原子最外层电子数少于4,所以最外层少于4的原子一定是金属元素原子(×)
2.下列对有关事实的解释中,错误的是( )
A. 氮元素和钠元素所属周期不同——最外层电子不同
B. 硫和磷的元素种类不同——质子数不同
C. 冰水共存物属于纯净物——冰和水都由水分子构成
D. 硫在空气和氧气中燃烧的火焰颜色不同——氧气浓度不同
【答案】A
3.下列说法中,正确的是( )
A. 同种元素组成的物质性质一定相同
B. 同一种元素可以组成不同种单质
C. 含氧元素的物质一定是氧化物
D. 只含有一种元素的物质一定是纯净物
【答案】B
4.下列事实的结合或解释正确的是( )
A. 搅拌能加快蔗糖在水中的溶解:搅拌能使蔗糖分子在水中溶解更多
B. 分离液态空气制氧气,说明分子可以再分
C. 水银温度计中水银受热体积变大:说明分子之间间隔受热变大
D. 酒香不怕巷子深:说明分子在不断运动
【答案】D
5.(2018·甘肃)元素观、做粒观是化学的重要观念。下列有关元素和做粒的说法不正确的是( )
A.分子、原子和离子都是成物质的粒子
B.同种元素的原子核内质子数与中子数一定相等
C.元素的原子序数与该元素原子核电荷数在数值上相同
D.在物质发生化学变化时,原子的种类不变,元索的种类也不会改变
【答案】B
九、化学教材实验
1.下列是有关课本实验的一些说法,判断对错
(1) 测定空气中氧气含量的实验中,可以用足量的硫替代红磷(×)
(2) 用过氧化氢溶液制取氧气实验中,可以用硫酸铜溶液替代二氧化锰作催化剂 (√ )
(3) 实验装置的组装顺序要遵循“从左到右、从上到下”的原则,拆卸装置刚好相反 (×)
(4) 制取气体时,若装置的气密性不好,则收集不到气体或始终收集不满(√)
(5) 测定空气中氧气含量的实验中,若燃着的红磷伸入集气瓶的速度太慢,则测定结果偏高(√)
(6) 制备气体时,先装药品,后检查装置的气密性(×)
(7) 用滴管取细口瓶中的液体时,先将其伸入液体内,后挤压取液(×)
(8) 用托盘天平称量10g固体药品时,先放砝码,后放药品(√)
(9)加热KMnO4并用排水法收集O2,实验结束时先熄灭酒精灯,后移出导管(×)
(10) 吸水性的物质都需密封保存,需要密封保存的物质都有吸水性(×)
(11) 要粗略地测定空气里氧气的含量,可用铁丝代替红磷在空气中燃烧(×)
(12) 排水法收集O2,导气管口有气泡连续均匀的冒出时开始收集,收集到的O2更纯净(√)
(13) 电解水生成氢气和氧气——证明水是由氢分子、氧分子构成的(×)
2.(2018·四川)回答下列问题。
(1)从宏观角度看,水是由 组成的;
(2)从微观角度看,水是由 构成的,每个水分子都是由 构成的,保持水化学性质的最小粒子是 。
(3)填写下列表格。
基本反应类型
化学方程式
反应应用
化合反应
CaO H2O=Ca(OH)2
分解反应
验证水的组成
【答案】(1)氢元素和氧元素(或H、O)(2)水分子(或H2O);2个氢原子和1个氧原子;水分子(或H2O);(3)做干燥剂或制取熟石灰;2H2O=(通电)2H2↑ O2↑。
3.(2018·江西)根据下列图示,回答相关问题
(1)实验一:实验中铜片上出现的现象是_____________,该反应的化学方程式是_______。
(2)实验二:自制建议净水器中小卵石,石英秒和蓬松棉的作用是__________。
【答案】(1)红色固体表面逐渐变黑,2Cu O2=(△)2CuO (2)过滤
十、气体的制备
1.(2018·四川)(4分)请结合下列实验装置,回答问题:
(1)以高锰酸钾为原料、利用A装置制取氧气的化学方程式为 。
(2)用石灰石和稀盐酸制取并收集二氧化碳,选用的装置为 (填字母)。
要制取4.4g二氧化碳,需要含杂质20%的大理石 g。
(3)与集气瓶配套使用的玻璃片一般一面为光滑面,另一面为磨砂面,收集气体时用玻璃片的 盖好集气瓶(填“光滑面”或“磨砂面”)。
【答案】(1)以高锰酸钾为原料、利用A装置制取氧气的化学方程式为 2KMnO4K2MnO4 MnO2 O2↑。
(2)用石灰石和稀盐酸制取并收集二氧化碳,选用的装置为 BD(填字母)。
CaCO3 2HCl=CaCl2 H2O CO2,
100 44
x×(1﹣20%) 8.8g x=12.5g;
(3)与集气瓶配套使用的玻璃片一般一面为光滑面,另一面为磨砂面,收集气体时用玻璃片的 磨砂面 盖好集气瓶(填“光滑面”或“磨砂面”)。
2.(2018·甘肃平凉)结合下列化学实验装置,回答有关问题。
(1)写出图中标有宇母的仪器的名称:a ;
(2)实验室用氯酸钾制取氧气应选择的发生装置是 (填代号),可用 法收集氧气。制得的氧气用来做如右下图所示的实验,发现H中铁丝不燃烧,其原因是 。写出G中反应的化学方程式 ;
(3)实验室制取二氧化碳常用的药品是 ,若用装置E收集二氧化磯,则 气体应从填“①”或“②")端进入;若要获得干燥的二氧化,可将装置B和装置D用胶皮管连接,并在装置D中盛放 (填物质名称}试剂。
(4)实验室常用装置C代替装置B制取气体,装置C的优点是 。
【答案】(1)试管(1分) 锥形瓶(1分)
(2)A(1分) 排水(或向上排空气)(1分)
H中铁丝的温度未达到着火点(1分) 3Fe 2O2 Fe3O4(2分)
(3)大理石(或石灰石)与稀盐酸(2分) ①(1分) 浓硫酸(1分)
(4)可以随时控制反应的发生与停止(2分)
3.实验室制取气体的装置如图所示,根据所学的知识回答下列问题。
(1)图中仪器a的名称是________________;
(2)实验室用过氧化氢溶液和二氧化锰制氧气,该反应的表达式是______________________,从图中选择仪器组成制取装置,若选择了a.b.d.g.h.i.j 还要选择________;若用该装置收集氧气,验满的方法是________________________。
(3)某同学把少量高锰酸钾加入氯酸钾中加热时,发现会很快产生氧气,他认为高锰酸钾是氯酸钾分解的催化剂,小明认为他的观点不对,理由是________________________(用化学表达式解释);
(4)小明用家里的小针筒和废药瓶组成一套微型装置(如图所示)替代装置上述装置,得到老师的表扬,用该装置做实验的优点是________(填序号)
①节约药品用量 ②产生的气体不含任何杂质 ③能完全消除废液排放 ④能控制液体的滴加速度
【解析】(1)根据实验室常用仪器可知a为锥形瓶;(2)实验室用过氧化氢溶液和二氧化锰制取氧气,化学反应方程式如上;从图中选择仪器组成制取装置,若选择了a、b、d、g、h、i、j 还要选择c、n;向上排空气法收集氧气要验满,验满时要用带火星的木条,并将其放到集气瓶瓶口,如果复燃,则证明已满;(3)由于高锰酸钾在加热时能够发生分解反应,化学反应方程式为如上 ,这样在氯酸钾在受热时高锰酸钾分解出的MnO2就能够对氯酸钾的分解起到催化的作用,这个过程中高锰酸钾转化为二氧化锰的等物质,其中的二氧化锰改变了氯酸钾的分解速率,所以作催化剂的是二氧化锰,而非高锰酸钾。从概念的角度,催化剂是质量和化学性质都不改变的物质,在这里,高锰酸钾分解了,那么本身的化学性质改变,自身分解了,质量当然也就发生了改变,即高锰酸钾在反应前后质量和化学性质都发生了改变。所以高锰酸钾不是该反应的催化剂。(4)装置改进后的优点是:操作简便;节约药品用量;能控制液体的滴加速度,从而能够控制反应的进行。
4.结合下列图示实验装置,回答有关问题:
(1)仪器a的名称是______;实验时使用它的优点是_____________。实验室用双氧水制取O2时,应选择的发生装置是______(填字母,下同)和收集装置是 _____ ,化学反应方程式为__________________,该反应属于_______反应。
(2)常温下,硫化氢(H2S)是一种有臭鸡蛋气味的气体:验室可用硫化亚铁(FeS)固体和稀硫酸反应制得,该反应的方程式为FeS H2SO4=H2S↑ FeSO4.实验室制取硫化氢气体应选用的发生装置是________(填字母),依据是___________________。
(3)实验中采用排水法收集氧气,当实验即将结束时,如果先熄灭酒精灯,且水槽中的水开始沿着导管倒流,此时的应急处理操作是__________________________。
(4)实验室采用A装置制取氧气,化学反应方程式为__________________________。
【答案】 (1) 长颈漏斗 添加液体方便 B C 2H2O2
2H2O O2↑ 分解; (2) B 固体液体常温制气体; (3) 拔掉胶塞或重新点燃酒精灯; (4)2KMnO4
K2MnO4 MnO2 O2↑
,
免责声明:本文仅代表文章作者的个人观点,与本站无关。其原创性、真实性以及文中陈述文字和内容未经本站证实,对本文以及其中全部或者部分内容文字的真实性、完整性和原创性本站不作任何保证或承诺,请读者仅作参考,并自行核实相关内容。文章投诉邮箱:anhduc.ph@yahoo.com