大学化学配位化合物的化学键理论(C博士专栏)
更多消息,请关注公众号--“康桥电池能源CamCellLab”
C博士专栏 ,专注于电池电化学领域的博士及专家们的专栏。本栏目特邀请公众号“康桥电池能源CamCellLab”的特约撰稿人查尔斯博士,他多年从事电池电化学方面的研究工作。去年他在本公众号开专栏,介绍电池知识,获得很好的反响。今年他开始介绍一些大学化学知识,非常精彩,看内容!

图1:分子的球棍模型
参与化学成键的电子是价电子,对于大多数原子来说,价电子是占据最外层电子层中的电子。美国化学家刘易斯(G. N. Lewis,1875–1946)提出了一种简单的方法来显示原子中的价电子并在键形成过程中跟踪它们,这种方法现在叫做刘易斯符号(Lewis Symbols)。
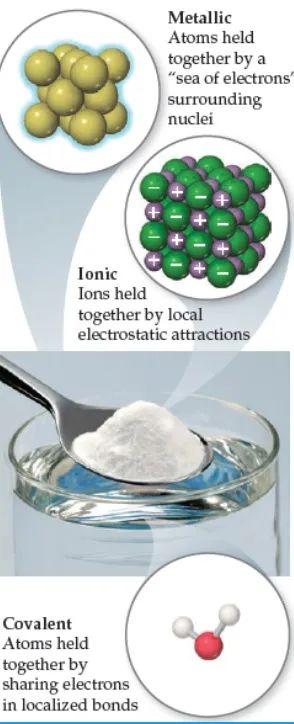
图2:离子键、共价键和金属键。三种不同物质通过不同类型的化学键结合在一起。
每当两个原子或离子牢固地结合在一起时,我们就说它们之间存在化学键。化学键一般分为三种类型:离子键、共价键和金属键。这三种类型的键在图2 所示的物质中:我们使用不锈钢勺子将食盐加入水中。
食盐是氯化钠,NaCl,由钠离子Na 和氯离子Cl-组成。氯化钠由离子键结合在一起。离子键是由于带相反电荷的离子之间的静电吸引力而形成的。
水主要由 H2O 分子组成。氢原子和氧原子通过共价键连接,其中分子是通过原子之间共享电子而形成的。
这些不同的物质,盐,水和铁,由于它们的组成原子相互连接的方式不同,它们的性质也不同。可以表现在:盐很容易溶于水,但铁金属不会。
下期剧透:刘易斯符号(Lewis Symbols)和八电子稳定结构规则(Octet Rule)
,免责声明:本文仅代表文章作者的个人观点,与本站无关。其原创性、真实性以及文中陈述文字和内容未经本站证实,对本文以及其中全部或者部分内容文字的真实性、完整性和原创性本站不作任何保证或承诺,请读者仅作参考,并自行核实相关内容。文章投诉邮箱:anhduc.ph@yahoo.com






