植物胶表观粘度(分子胶的下一程)
我们目前依然不能对感兴趣的靶点进行定向的分子胶降解剂的理性设计。 但是在过去两年内,我们对潜在可降解底物结构特征的了解不断深入,在分子胶药化性质的优化以及基于诱导结合或降解的高通量筛选技术方面都取得了长足的进步,直接推动了多个分子胶化合物和降解靶点的发现和临床前研究。
——达歌生物仓勇教授
上世纪50年代末至60年代初,全球46个国家的医生将沙利度胺用于治疗妊娠期妇女的孕吐。当时,这种药物被认为是安全的。1961年,医学界发现子宫内的沙利度胺暴露量直接与婴儿严重的生理缺陷有关,这种药物直接导致数千名儿童的四肢畸形和其他损伤。同一年,该药从绝大多数国家的市场撤出。
1964年,一名医生将沙利度胺用于治疗患有皮疹等炎症性并发症的麻风病患者,几天内症状得到控制。沙利度胺的这种活性促使研究人员对其进行更深入的研究。1994年,研究人员发现它可能具有干扰新血管生成的能力,这项发现让科学家进一步研究沙利度胺是否具有抗肿瘤活性。上世纪90年代后期,研究发现沙利度胺可以有效地治疗多发性骨髓瘤。
尽管当时研究人员还不知道沙利度胺导致海豹儿的具体机制,有科学家推测沙利度胺抗肿瘤与致畸的机制可能是相同的。后来,科学家才发现沙利度胺是一类分子胶。分子胶是指一种可将两种蛋白“粘贴”到一起的小分子药物。最常见的分子胶是将致病蛋白与蛋白降解酶结合,随后以泛素化方式诱导蛋白降解。

分子胶(粉色)与 E3 连接酶cereblon(绿色)结合,以不同的方式改变其表面以招募不同的蛋白质靶标(来源:达歌生物)
沙利度胺导致海豹儿的作用通路可能有很多,但其中一种是破坏了胎儿生长发育必须的蛋白质。而在治疗多发性骨髓瘤的过程中,沙利度胺同样是降解了导致疾病发生的关键蛋白。
哈佛大学化学生物学家、蛋白质降解领域的开拓者 Stuart Schreiber表示上世纪90年代科学家首次发现分子胶。Schreiber与人共同创办了美国麻省理工学院-哈佛大学的博德研究所及多家初创公司,其中包括分子胶公司 Magnet Biomedicine。
来源:Magnet Biomedicine
在研究几种天然产物如何发挥免疫抑制功能、预防器官移植排斥的研究中,Schreiber实验室博士后Jun Liu发现此类天然产物会导致两种蛋白质结合,从而阻断免疫信号通路。Schreiber说:“这几种天然产物结构非常复杂,有着出人意料的作用机制。”Schreiber首先在组会上创造了“分子胶”这个术语,并于1992年在Cell杂志上描述了这种现象。当时Schreiber认为:“化学家可能无法合成分子胶,这太复杂了,也许真的需要数十亿年的自然选择才能实现这一目标。”而Schreiber现在也承认,在这件事上他没有准确地预测未来。尽管发现分子胶存在困难,但科研人员和制药公司已经成功做到了这一点。
分子胶的兴起
事实上,意识到分子胶的开发难度很大后,Schreiber和同事Gerald Crabtree想到了一种变通方案:“为什么不找一种蛋白质配体和另一种蛋白质配体,然后通过化学方式将二者结合呢?”这也就是大名鼎鼎的蛋白水解靶向嵌合体(PROTAC)的由来。
近年来,PROTAC蓬勃发展。首篇PROTAC论文通讯作者CrAIg Crews创立的Arvinas公司在研管线进度最快,目前处于临床II期的两款药物分别用于治疗前列腺癌和乳腺癌(与辉瑞合作)。此外,Nurix Therapeutics、Kymera Therapeutics 和Foghorn Therapeutics等明星公司均有产品进入临床I期。
尽管PROTAC很有前景,但是过大的分子量限制了自身的生物利用度。此外,PROTAC还要求靶蛋白有结合口袋,但是很多致病蛋白并不满足这一条件。
分子胶有望克服这些障碍。加州大学伯克利分校的化学生物学教授Daniel Nomur 认为,分子胶的主要优势在于它可以将两个蛋白界面结合在一起形成结合口袋。单个蛋白质可能没有足够的结合位点。小分子将两种蛋白距离拉近后,可以创造足够的结合口袋,足以与分子胶发生相互作用。因此,这种策略可以让更广泛的无法成药蛋白成为药物开发的靶标。
Schreiber说,今年分子胶的爆发不存在标志性的时点。新工具的出现推动了该领域的进步,但这是过去30年努力的一砖一瓦不断搭建的结果。
摆脱困境
开发分子胶不是一件容易的事,目前很多分子胶(包括沙利度胺)都是偶然发现的,必须要找到理性开发设计策略才能确保该领域的长久发展。
BMS公司获FDA批准的代表性分子胶
来源:医药魔方NextPharma
2006年,Celgene公司申报的以沙利度胺治疗多发性骨髓瘤适应症获批;同年沙利度胺类似物来那度胺的多发性骨髓瘤适应症获批。2013年,FDA批准了对多发性骨髓瘤疗效更强的泊马度胺。2019年,BMS收购了Celgene,以此扩大在分子胶领域的商业版图。BMS旗下自Celgene收购而来的临床试验阶段的分子胶如下表。BMS收购的这些分子胶候选化合物证明了系统开发策略的可行性。
BMS部分在研分子胶
来源:医药魔方NextPharma
目前,绝大多数从事分子胶开发的公司都致力于通过混合和匹配经典药物发现方法来寻找候选化合物。达歌生物首席执行官邹丽晖博士表示,公司采用三种方法开发分子胶。
第一种方法是表型筛选,以候选药物测试对肿瘤细胞的杀伤功能。如果候选药物确认以E3连接酶依赖的方式杀伤肿瘤细胞,研究人员将进一步探索被降解的蛋白质,同时确认该药物是以分子胶的作用模式发挥杀伤作用的。巴塞罗那生物医学研究所靶向蛋白质降解专家 Cristina Mayor-Ruiz表示,这种筛选方式无异于大海捞针,需要建立一个细胞实验平台,进行海量实验找到预期分子。
第二种方法是利用质谱法研究候选药物处理细胞时,蛋白质组学将发生什么变化。例如,向含有E3连接酶CRBN的细胞中引入候选分子胶,对照组不做处理。如给药细胞中出现蛋白水平下调,则需要进一步确认是由于分子胶作用机理导致的。
第三种方式是利用人工智能(AI)预测哪些蛋白可能容易被分子胶降解,随后针对该靶点开发分子胶药物。有些公司特别重视AI在分子胶开发过程中的作用。Triana Biomedicines利用深度学习算法,根据靶蛋白表面特征寻找合适的E3连接酶;Monte Rosa Therapeutics则使用AI驱动的深度神经网络鉴别潜在靶蛋白表面可被E3连接酶识别的表面特征。
尽管不同的公司有许多开发分子胶的方法,但不同于PROTAC的理性设计,分子胶还不能实现从头开发。Monte Rosa的首席执行官 Markus Warmuth认为,没有一种分子胶水可以完全从零开始制造:“事实上,只有在你知道点什么的情况下你才能进行设计。对我而言,这有点像已知一个核心结构,对该结构进行有意义的结构修饰。”而经典的药物发现是合成数百万个分子,以“分子轮盘赌”的方式看哪种药物结构有效。
2022年分子胶相关融资事件
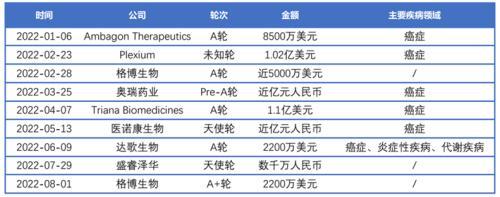
数据截至2022年8月,来源:医药魔方PharmaInvest
无论这些公司最终能否开发出分子胶药物,它们都已经获得了资本市场的认可。达歌生物6月9日完成了2200万美元A轮融资;Triana Biomedicines于4月7日完成1.1亿美元的A轮融资;而在去年6月24日,Monte Rosa Therapeutics完成IPO,募资总额达到2.223亿美元。
大型制药公司也对这个赛道十分看好。BMS除了收购Celgene介入分子胶领域外,还加强对外合作。今年5月,BMS向CRO公司Evotec支付2亿美元,将双方在分子胶领域的合作延长8年;6月,BMS还与一家总部位于维也纳的分子胶公司Proxygen达成总额为5.54亿美元的合作伙伴关系。
除了BMS的几款临床试验阶段的分子胶外,还有多个分子胶处于临床阶段。Novartis的NVP-DKY709处于临床I期;Bayer与Broad Institute合作开发的BAY 2666605也处于临床I期,适应症包括转移性黑色素瘤、晚期实体瘤。C4 Therapeutics是一家从丹娜法伯癌症研究院分离出来的初创公司,目前有一款分子胶和一款PROTAC处于临床I期。
C4 的首席科学官 Stew Fisher 在谈到 PROTAC 和分子胶时表示:“我们不想成为一家专注于PROTAC或者分子胶的公司。”该公司的战略决策是重点针对研究较为透彻的E3 连接酶成分CRBN,开发最为合适的靶蛋白降解剂,无论是哪种药物形式。
值得一提的是,尽管分子胶的热度提升,但没有迹象表明PROTAC的开发趋势在放缓,有大量PROTAC项目已经进入临床开发阶段。伯克利科学家、企业家Nomura表示:“PROTAC的设计是模块化的,我认为它们会长期存在。但是分子胶类药性更优,如果我们有系统发现的策略,我认为分子胶将在药物发现领域站稳脚跟。”

PROTAC与分子胶临床在研对比(来源:医药魔方NextPharma)
分子胶的下一程
目前,分子胶的主要功能是降解蛋白质,但理论上分子胶可以将任意两种蛋白质结合到一起。一些公司不希望分子胶发挥蛋白降解的功能,正在探索E3连接酶以外的蛋白。
Generian Pharmaceuticals最近与Astellas Pharma 的子公司合作,开发可以激活和稳定蛋白靶标的小分子药物。Generian首席执行官 Hank Safferstein表示,公司产品管线包括随年龄增长表达下调的蛋白稳定类药物。
分子胶领域的更高目标应该是建立为任意蛋白开发分子胶的理性设计策略。曾在Monte Rosa工作过的分子胶专家Shanique Borteley Alabi表示:“两个蛋白质,我要把它们‘粘’起来,这不是五年十年的事,我们还有很多要了解的地方,但是我认为我们可以做得更好。”
专家点评
上海科技大学生命科学与技术学院教授
达歌生物 联合创始人兼首席科学家
仓勇 博士

仓勇(Yong Cang)博士是上海科技大学生命科学与技术学院教授,也是达歌生物的联合创始人。他是蛋白泛素降解领域的专家,专注研究新型分子胶药物的筛选和机制,以及其在肿瘤靶向治疗和免疫治疗中的应用。他获得复旦大学生物化学本科学位,爱因斯坦医学院分子遗传学博士,在哥伦比亚大学完成博士后训练,并曾担任桑福德伯纳姆医学研究所助理教授和浙江大学教授。
医药魔方Pro:2020年8月,您在接受我们采访时曾提到,当时缺乏有效的手段来系统性筛选全新的分子胶化合物。两年过去了,分子胶目前的研发现状是怎样的?这项技术是否开始走向理性设计?
仓勇教授:我们目前依然不能对感兴趣的靶点进行定向的分子胶降解剂的理性设计。但是在过去两年内,我们对潜在可降解底物结构特征的了解不断深入,在分子胶药化性质的优化以及基于诱导结合或降解的高通量筛选技术方面都取得了长足的进步,直接推动了多个全新分子胶化合物和降解靶点的发现和临床前研究。
医药魔方Pro:理论上分子胶可以用于治疗任何疾病。然而,目前在研药物的适应症主要集中于肿瘤和自身免疫性疾病。造成这种现象的原因是什么?分子胶技术拓展到其他疾病领域有哪些挑战需要克服?
仓勇教授:主要有两个原因:第一,目前在研分子胶药物的靶点都是通过探索分子胶化合物而发现的,而不是基于感兴趣的靶点筛选或设计来的,这些靶点的生物学决定了现有药物的适应症集中在肿瘤和免疫疾病;第二,历史上,FDA批准了分子胶Thalidomide治疗麻风结节性红斑(erythema nodosum leprosum), Lenalidomide治疗多发性骨髓瘤,这些先驱药物在免疫疾病和癌症患者中已证明了它们的安全性、有效性,从而增强了药企对在研分子胶药物治疗这些适应症的信心。
分子胶结合泛素酶形成非自然的界面从而促进新蛋白的结合和降解,这种独特的作用机制也决定了分子胶的底物选择性会低于小分子抑制剂,所以分子胶药物的安全性和有效性往往决定于治疗窗口内靶向降解底物对适应症的调控程度及重要性。对于慢性病,如神经退行性疾病和代谢疾病,我们需要建立能够有效评估分子胶药物降解体内蛋白所导致的长期后果的方法。
医药魔方Pro:据统计,2022年上半年,全球分子胶相关融资事件数量高于PROTAC。对于今年上半年分子胶“融资热度”赶超PROTAC,您怎么看?
仓勇教授:大多数不可成药靶点,比如转录因子和RNA结合蛋白,都没有化合物配体(ligands), 从而给PROTAC的设计带来挑战,而分子胶不需要这些配体就可以诱导降解这些靶点,虽然如何发现这些分子胶是另一个层面的挑战。另外,分子胶分子量小,成药性更高,甚至可以穿透血脑屏障,所以相比PROTAC,有更大的概率能克服现有小分子抑制剂药物的限制,给患者提供前所未有的治疗手段。
医药魔方Pro:有观点认为,分子胶短期内可能不会有重大突破,对此您有怎样的解读?
仓勇教授:Craig Crews在2013年成立Arvinas公司,当时很多人认为PROTAC就是学术研究的一个有趣的工具,不可能成为药物。后来随着研究的深入,技术的革新和资本的投入,现在大家开始笑话那些早些时候笑话PROTAC的人。
医药魔方Pro:达歌生物在今年6月完成了2200万美元的A轮融资。目前,公司在研管线进展如何?能否介绍一下未来3-5年的开发计划?
仓勇教授:达歌生物所有的分子胶管线都是First in class,药物筛选验证,化合物优化,药理毒理和临床适应症都由自己独立产生的数据来指导。公司的代表性项目包括:1)降解RNA结合蛋白的口服分子胶药物,已经接近PCC,将用于治疗表达特定生物标志物的结直肠癌和其他实体瘤,包括脑瘤(该分子胶可以进脑);2)降解细胞周期检查点WEE1的口服分子胶药物,将用于治疗表达特定生物标志物的一类罕见儿童癌症,已有证据显示,这类候选分子胶单药比WEE1抑制剂更加有效;3)GSPT1降解剂,公司正在和跨国药厂合作,探索这类分子作为ADC药物弹头(payload)的应用。
开发计划方面,公司计划今年年底前确认一个PCC,明年年底之前递交IND,并确定第二个PCC,2024年启动临床I期。在BIO会议后,达歌生物受到很多制药公司的关注,现在正在探讨基于达歌分子胶平台的科研合作以及现有管线的共同开发。
本文源自医药魔方
,免责声明:本文仅代表文章作者的个人观点,与本站无关。其原创性、真实性以及文中陈述文字和内容未经本站证实,对本文以及其中全部或者部分内容文字的真实性、完整性和原创性本站不作任何保证或承诺,请读者仅作参考,并自行核实相关内容。文章投诉邮箱:anhduc.ph@yahoo.com






