芳香性怎么判断的(芳香研究有多香)
1931年,德国化学家Erich Hückel发表了一篇在化学史上具有里程碑意义的论文,这篇论文为以他名字命名的4n 2环烯芳香性规则——Hückel规则——埋下了伏笔。然而,当时这位斯图加特工业大学编外讲师的理论太过超前,并不被绝大多数化学家所认可,直到20年后,情况才得以改观。时至今日,“什么是芳香性”依然是化学研究中最具争议、也最吸引人的问题之一。近日,西班牙赫罗纳大学的Miquel Solà教授在Nature Chemistry 上撰文,简要回顾了芳香性研究中那些经典而有趣的历史。

图1. 德国化学家Erich Hückel。图片来源于网络
Hückel规则。即4n 2π电子规则(n为整数),基于Hückel的分子轨道(MO)理论。对于一个具有闭壳(closed-shell)结构、简并分子轨道、DNh对称的单环烯(annulenes, CnHn)来说,若π电子数符合4n 2(n为整数),那么分子具有芳香性;若π电子数符合4n(n为整数),则分子具有反芳香性(图2)。1954年,Doering和Knox合成了非六元环的芳香性环庚三烯基阳离子(C7H7 ),其π电子数依然符合Hückel规则,是这一规则被成功证实的经典案例之一。

图2. 符合Hückel规则的六元苯环。图片来源:Nat. Chem.
开壳芳香性。值得注意的是,借助4n 2或4n π电子计数规则来判断环烯的芳香性或反芳香性依赖于分子的自旋状态和拓扑结构。针对处于第一激发三重态(T1)的环烯,Colin Baird 提出了Baird规则,在这种情况下,含4n π电子数的环烯具有芳香性,而含4n 2 π电子数则具有反芳香性,例如环丁二烯阳离子含4个π电子,具有Baird芳香性。2008年,Soncini和Fowler对Hückel规则和Baird规则进行了扩展,并考虑了奇偶数自旋态问题。随后,Mandado等人将Hückel规则、Baird规则和Soncini–Fowler规则融合成单一规则,总结为带有奇数(2n 1)个α和β电子的环烯具有芳香性,而带有偶数(2n)个α和β电子的环烯具有反芳香性。例如环辛四烯含有奇数个α电子(5)和β电子(3),具有芳香性(图3)。但是,对于具有偶数个α电子和奇数个β电子(或相反)的环烯,却无法判断其芳香性。
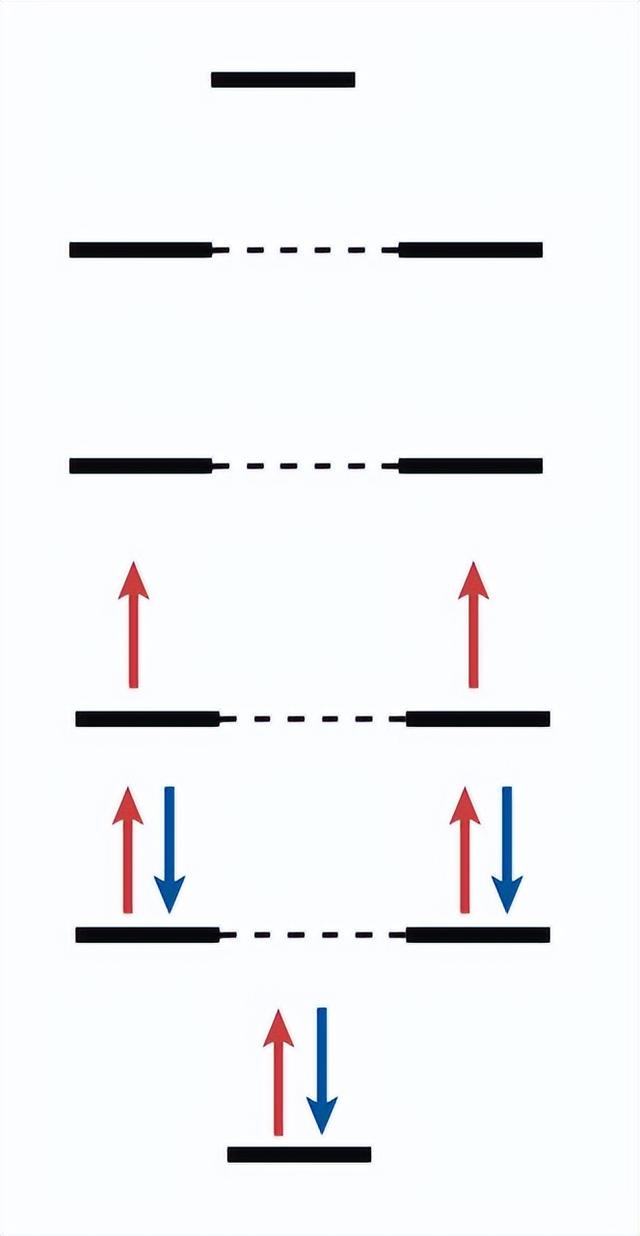
图3. 环辛四烯电子轨道分布(红色为α电子,蓝色为β电子)。图片来源:Nat. Chem.
分子拓扑学。另一个迷人的现象是莫比乌斯(Möbius)芳香性,它存在于具有Möbius带的环状共轭化合物中。1958年,Craig和Paddock首次从理论上描述了有机金属体系的Möbius芳香性,6年后Heilbronner进一步阐述了环烯结构的Möbius芳香性。在单环Möbius芳香化合物中,闭壳芳香电子构型含4n π电子。2003年,Ajami、Herges及其合作者第一次合成出稳定的Möbius芳香化合物。4年后,Stępieńet等人合成了第一个动态Hückel–Möbius型化合物(图4),它的Möbius构象具有一个8字形单捻结构。在金属芳香环烯中,含Möbius芳香性并不需要加入扭曲分子结构(即所谓的Craig–Möbius芳香性)。随后,Ottosson 等人基于环烯的π电子数(4n vs. 4n 2)、拓扑结构(Hückel vs. Möbius)和电子态(S0 vs. T1/S1)构建了“芳香性立方体(aromaticity cube)”。最近,化学家通过获取连接数(Lk,表示环烯的缠绕次数(包括扭曲和扭转))实现了Hückel和Möbius两大规则的统一(图4),即含偶数Lk的环烯烃符合Hückel规则,含奇数Lk则符合Möbius规则。

图4. Möbius芳香化合物电子轨道(a),动态Hückel–Möbius型化合物(c),芳香性立方体(d),环烯扭曲和扭转示意图(e)。图片来源:Nat. Chem.
金属芳香性和多环芳烃芳香性。在过去的几十年里,4n 2和4n芳香性规则已扩展到金属有机、全金属和半金属化合物中,并且这些化合物具有“多重芳香性”。例如Li3Al4–金属簇中的Al4–环具有π-Baird芳香性(4π-电子),σr- 径向和σt–切向则是Hückel芳香性(σr- 和σt–轨道上均含2个电子)。而对于多环芳烃(PAHs)的芳香性,Platt率先尝试应用Hückel规则,他将多环芳烃分为外周和内核两部分,并以外周π-电子数来判断芳香性,例如芘的外围有14个π-电子,具有芳香性。然而,Platt规则却无法应用于非苯型多环共轭烃(PCHs)。1972年,Clar提出π-六规则,认为芳香性是六元环在化合物中的局部属性,例如下图中菲红色结构要比蓝色结构多一个π-六环,这意味着依据Clar规则,红色结构更真实的描述了菲的分子结构和芳香性(图5)。
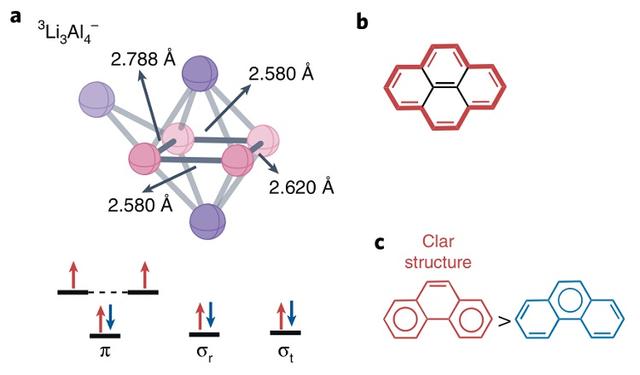
图5. Li3Al4–金属簇结构示意图(a),Platt规则判断芘芳香性(b),Clar规则判断菲芳香性(c)。图片来源:Nat. Chem.
Clar规则的另一个替代选择是Fries规则,此规则认为化合物倾向于含最大数量的Fries六元环(环上含六个π-电子)。1984年,Glidewell和Lloyd 对Clar规则进行扩展,他们认为非苯多环共轭烃(PCHs)的总π-电子数倾向于形成最小的4n 2组,避免形成最小的4n组。例如依据Glidewell–Lloyd规则,图中二环癸烷[6.2.0]戊烯的红色共振结构(含有一个小的2π-电子环和一个大的8π-电子环)比蓝色共振结构(含有一个小的4π-电子环和一个大的6π-电子环)更合理。有趣的是,Baird和Clar规则组合起来能够解释线性二苯并[b,h]联苯和扭结二苯并[a,i]联苯的稳定性差异,这是因为后者含Baird-芳香-π-四元环,因此扭结异构体更稳定(图6)。
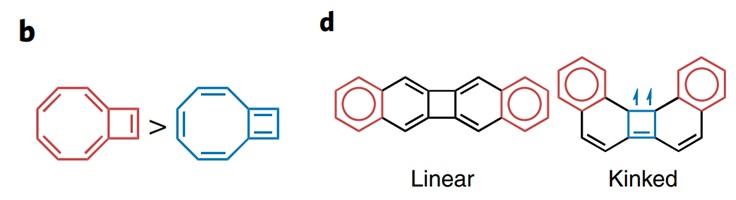
图6. 二环癸烷[6.2.0]戊烯的红色和蓝色共振结构(b),线性和扭结二苯并[b,h]联苯(d)。图片来源:Nat. Chem.
三维芳香性。1959年,Lipscomb等人用X-射线衍射分析确定了B10H102-的离子结构。3年后,Muetterties等人首次合成了十二氢十二硼酸盐[B12H12]2-和十氢十二硼酸盐[B12H10]2-衍生物,并引入了三维芳香性概念。对于具有三维立体结构的硼烷和碳硼烷簇的芳香性(反芳香性),可以通过Wade–Mingos规则进行判断,即Wade 2N 2和Mingos 4N 2 电子规则(其中N表示多面体的顶点数)。然而,Wade–Mingos规则无法判断稠合型多面体硼烷(例如[B12H10]2–)的芳香性,为此Jemmis等人针对这类化合物提出了mno 规则,即所需电子数 = m n o,其中m为多面体数,n为骨架原子总数,o为共用顶点数。此外,Wade–Mingos规则也无法应用于3D球型芳香化合物(例如一些带电富勒烯),针对这类化合物提出了Hirsch 2(N 1)2芳香性判断规则。此规则认为,近似球形化合物的π-电子可以视为均匀环绕球形表面的电子气。与此类似,质谱中观察到的碱金属、碱土金属和金簇的电子分布也可以用球状jellium模型进行阐释(图7)。
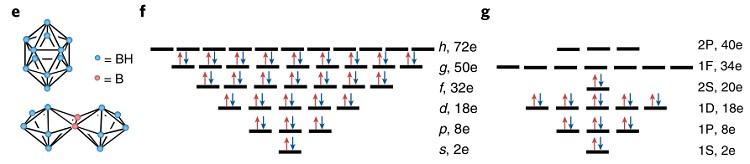
图7. [B12H12]2-和[B12H10]2–分子结构(e),C60 10和Na20分子轨道示意图(f,g)。图片来源:Nat. Chem.
在一些分子量大的圆柱形分子中(例如纳米管、环对苯撑或某些硼和氮化硼团簇),芳香性可以通过空心圆柱模型(HCM)进行描述。属于这类空心圆柱模型(HCM)的化合物分子轨道可以分为径向和切向(图8),两个方向符合4n 2m芳香规则(其中n和m分别代表简并和非简并分子轨道数量)。

图8. 圆柱形分子芳香性分子轨道。图片来源:Nat. Chem.
然而,有些化合物并不能简单地归类为Hückel或Baird芳香性,这是因为它们是两者的组合。例如TMTQ在单线态基态(S0)时具有醌型结构(图9a左),而在T1态的高稳定性则可以通过中心环的Baird芳香性(即M10A2 具有8π电子,图9a右)或Hückel芳香性(即闭壳10π电子,图9a中)来解释,同时计算结果表明在TMTQ的T1(和S1)态下的M10A环约为85% Hückel和15% Baird。另外,还有一些化合物具有混合Hückel-Möbius特征(如IrI(C5H5)(PPh3)2),并且Hückel和Craig-Möbius芳香性的贡献不同(图9b)。
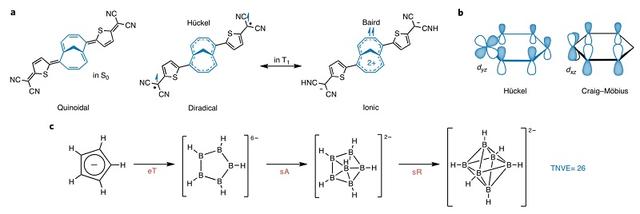
图9. 组合规则。图片来源:Nat. Chem.
自Hückel规则首次提出以来,围绕着芳香性的研究一直被大家所关注,所有的进步都在促进统一芳香性的理论完善,这反过来将有助于更好地理解化学中的这一关键概念以及芳香性对分子反应性的影响。
Aromaticity rules
Miquel Solà
Nat. Chem., 2022 14, 585–590, DOI: 10.1038/s41557-022-00961-w
(本文由天生西南供稿)
,免责声明:本文仅代表文章作者的个人观点,与本站无关。其原创性、真实性以及文中陈述文字和内容未经本站证实,对本文以及其中全部或者部分内容文字的真实性、完整性和原创性本站不作任何保证或承诺,请读者仅作参考,并自行核实相关内容。文章投诉邮箱:anhduc.ph@yahoo.com